Phản ứng thuận nghịch là một khái niệm quan trọng trong hóa học, nơi mà các sản phẩm của phản ứng có thể quay trở lại và tái tạo thành các chất phản ứng ban đầu. Điều này không chỉ thể hiện tính linh hoạt của các phản ứng hóa học mà còn mở ra nhiều cơ hội áp dụng trong đời sống thực tiễn, từ công nghiệp đến sinh học. Qua bài viết này, hóa chất Đông Á sẽ đem đến cho các bạn cái nhìn sâu sắc hơn về phản ứng thuận nghịch, từ khái niệm cơ bản đến các ứng dụng sinh động trong cuộc sống hàng ngày.
Khái niệm về phản ứng thuận nghịch là phản ứng gì?
Phản ứng thuận nghịch là một loại phản ứng hóa học đặc biệt, trong đó các chất tham gia phản ứng không chỉ chuyển hóa thành sản phẩm mà các sản phẩm này còn có thể kết hợp trở lại để tạo thành chất ban đầu. Nói cách khác, phản ứng xảy ra theo cả hai chiều: từ trái sang phải (phản ứng thuận) và từ phải sang trái (phản ứng nghịch).
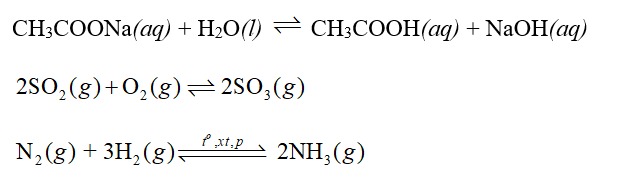
Một ví dụ minh họa về phản ứng thuận nghịch
Hình dung phản ứng thuận nghịch
Hãy tưởng tượng một con đường hai chiều. Xe có thể di chuyển từ điểm A đến điểm B (phản ứng thuận) và cũng có thể di chuyển từ điểm B về điểm A (phản ứng nghịch). Tương tự, trong phản ứng thuận nghịch, các chất hóa học cũng "di chuyển" qua lại giữa chất phản ứng và sản phẩm.
Biểu diễn phản ứng thuận nghịch
Để biểu diễn một phản ứng thuận nghịch, chúng ta sử dụng dấu mũi tên hai chiều (⇌) thay vì dấu mũi tên một chiều (→) như trong phản ứng thường. Ví dụ:
aA + bB ⇌ mM + nN
Trong đó:
Ví dụ về phản ứng thuận nghịch
Đặc điểm chung của phản ứng thuận nghịch
-
Xảy ra đồng thời theo hai chiều: Chất phản ứng biến đổi thành sản phẩm và ngược lại.
-
Có thể đạt đến trạng thái cân bằng: Khi tốc độ phản ứng thuận bằng tốc độ phản ứng nghịch.
-
Bị ảnh hưởng bởi các yếu tố: Nồng độ, áp suất, nhiệt độ, chất xúc tác.
Các yếu tố ảnh hưởng đến Phản ứng Thuận Nghịch
Phản ứng thuận nghịch là một quá trình liên tục, trong đó chất phản ứng biến đổi thành sản phẩm và ngược lại. Sự cân bằng của phản ứng này có thể bị ảnh hưởng bởi một số yếu tố sau:
Có nhiều yếu tố ảnh hưởng tới phản ứng thuận nghịch
1. Nồng độ:
-
Tăng nồng độ chất tham gia: Cân bằng sẽ chuyển dịch theo chiều làm giảm nồng độ chất đó, tức là theo chiều thuận.
-
Giảm nồng độ chất tham gia: Cân bằng sẽ chuyển dịch theo chiều làm tăng nồng độ chất đó, tức là theo chiều nghịch.
-
Tăng nồng độ sản phẩm: Cân bằng sẽ chuyển dịch theo chiều làm giảm nồng độ sản phẩm, tức là theo chiều nghịch.
-
Giảm nồng độ sản phẩm: Cân bằng sẽ chuyển dịch theo chiều làm tăng nồng độ sản phẩm, tức là theo chiều thuận.
2. Áp suất:
3. Nhiệt độ:
-
Phản ứng tỏa nhiệt:
-
Phản ứng thu nhiệt:
4. Chất xúc tác:
Các loại phản ứng thuận nghịch
Phản ứng thuận nghịch là loại phản ứng hóa học xảy ra theo cả hai chiều: từ chất phản ứng tạo thành sản phẩm (phản ứng thuận) và từ sản phẩm trở lại thành chất phản ứng (phản ứng nghịch).
Dựa vào bản chất của các chất tham gia và sản phẩm, ta có thể chia phản ứng thuận nghịch thành một số loại sau:
Phản ứng thuận nghịch có thể phân chia thành nhiều loại
1. Phản ứng ion hóa:
2. Phản ứng giữa các chất khí:
3. Phản ứng trong dung dịch:
4. Phản ứng trong pha rắn:
5. Phản ứng trong tự nhiên:
Quy trình đạt cân bằng trong phản ứng thuận nghịch
Phản ứng thuận nghịch là quá trình mà các chất tham gia phản ứng liên tục chuyển hóa thành sản phẩm và ngược lại. Khi tốc độ của phản ứng thuận bằng tốc độ của phản ứng nghịch, hệ đạt đến trạng thái cân bằng động.
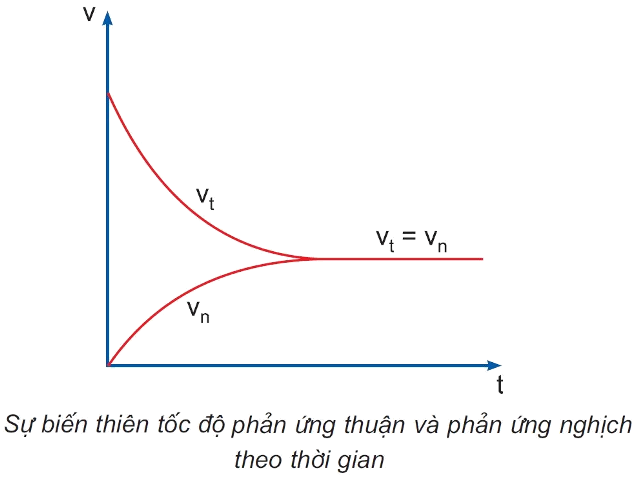
Quy trình đạt cân bằng trong phản ứng thuận nghịch
Quy trình đạt cân bằng:
-
Giai đoạn đầu:
-
Phản ứng thuận diễn ra mạnh mẽ hơn phản ứng nghịch.
-
Nồng độ chất tham gia giảm dần, nồng độ sản phẩm tăng dần.
-
Tốc độ phản ứng thuận giảm dần, tốc độ phản ứng nghịch tăng dần.
-
Giai đoạn cân bằng:
-
Tốc độ phản ứng thuận bằng tốc độ phản ứng nghịch.
-
Nồng độ các chất không đổi theo thời gian.
-
Hệ thống đạt trạng thái cân bằng động.
Đặc điểm của trạng thái cân bằng:
-
Cân bằng động: Các phản ứng vẫn tiếp tục xảy ra ở cấp độ phân tử nhưng tốc độ bằng nhau.
-
Tỷ lệ nồng độ: Tỷ lệ nồng độ các chất tại thời điểm cân bằng là một hằng số ở nhiệt độ xác định, gọi là hằng số cân bằng (Kc).
-
Tính thuận nghịch: Nếu tác động vào hệ cân bằng (thay đổi nồng độ, áp suất, nhiệt độ), cân bằng sẽ chuyển dịch theo chiều làm giảm tác động đó.
Phân tích sự chuyển hóa trong phản ứng thuận nghịch
Phản ứng thuận nghịch là một quá trình đặc biệt, trong đó các chất tham gia phản ứng không chỉ chuyển hóa thành sản phẩm mà các sản phẩm này còn có thể kết hợp trở lại để tạo thành chất ban đầu.
Quá trình chuyển hóa trong phản ứng thuận nghịch
1. Giai đoạn ban đầu:
-
Phản ứng thuận chiếm ưu thế: Khi phản ứng bắt đầu, nồng độ các chất tham gia thường cao hơn so với sản phẩm. Do đó, phản ứng thuận diễn ra nhanh hơn, tạo ra sản phẩm với tốc độ lớn.
-
Tốc độ phản ứng nghịch nhỏ: Vì nồng độ sản phẩm ban đầu thấp nên phản ứng nghịch diễn ra chậm.
2. Giai đoạn cân bằng:
-
Tốc độ hai phản ứng bằng nhau: Dần dần, khi nồng độ sản phẩm tăng lên, tốc độ phản ứng nghịch cũng tăng. Đến một thời điểm nhất định, tốc độ của phản ứng thuận bằng tốc độ của phản ứng nghịch.
-
Nồng độ các chất không đổi: Ở trạng thái cân bằng, nồng độ của các chất tham gia và sản phẩm không thay đổi theo thời gian.
-
Cân bằng động: Mặc dù nồng độ không đổi nhưng các phản ứng vẫn tiếp tục xảy ra ở cấp độ phân tử.
Các yếu tố ảnh hưởng đến sự chuyển hóa
-
Nồng độ: Tăng nồng độ chất tham gia sẽ làm tăng tốc độ phản ứng thuận và ngược lại.
-
Áp suất: Đối với phản ứng có chất khí tham gia, tăng áp suất sẽ làm cân bằng chuyển dịch theo chiều giảm số mol khí.
-
Nhiệt độ: Tăng nhiệt độ thường làm tăng tốc độ cả phản ứng thuận và nghịch, nhưng ảnh hưởng đến vị trí cân bằng phụ thuộc vào tính chất tỏa nhiệt hay thu nhiệt của phản ứng.
-
Chất xúc tác: Chất xúc tác làm tăng tốc độ cả phản ứng thuận và nghịch, giúp hệ đạt đến trạng thái cân bằng nhanh hơn nhưng không làm thay đổi vị trí cân bằng.
Ý nghĩa của sự chuyển hóa trong phản ứng thuận nghịch
-
Hiểu rõ bản chất của phản ứng: Giúp chúng ta hiểu rõ hơn về quá trình chuyển hóa giữa chất phản ứng và sản phẩm.
-
Dự đoán chiều chuyển dịch của cân bằng: Khi điều kiện phản ứng thay đổi, chúng ta có thể dự đoán được chiều hướng của phản ứng.
-
Điều khiển phản ứng: Bằng cách thay đổi các yếu tố ảnh hưởng, chúng ta có thể điều khiển phản ứng theo hướng có lợi.
Ứng dụng của phản ứng thuận nghịch trong công nghiệp và nghiên cứu
Phản ứng thuận nghịch, với khả năng chuyển đổi linh hoạt giữa chất phản ứng và sản phẩm, đóng vai trò quan trọng trong nhiều lĩnh vực của cuộc sống, đặc biệt là trong công nghiệp và nghiên cứu.
Trong công nghiệp
-
Sản xuất hóa chất:
-
Tổng hợp amoniac: Phản ứng Haber-Bosch là một ví dụ điển hình về ứng dụng phản ứng thuận nghịch trong sản xuất amoniac, một nguyên liệu quan trọng cho ngành nông nghiệp và công nghiệp hóa chất. Bằng cách điều chỉnh nhiệt độ, áp suất và nồng độ, các nhà sản xuất có thể tối ưu hóa hiệu suất của quá trình này.
-
Sản xuất axit sulfuric: Quá trình tiếp xúc là một quá trình công nghiệp quan trọng để sản xuất axit sulfuric. Quá trình này liên quan đến nhiều phản ứng thuận nghịch, và việc điều khiển các cân bằng hóa học là rất quan trọng để đạt được hiệu suất cao.
-
Luyện kim: Nhiều quá trình luyện kim liên quan đến các phản ứng thuận nghịch. Ví dụ, quá trình khử oxit kim loại bằng carbon monoxide là một phản ứng thuận nghịch.
-
Chế biến thực phẩm: Quá trình lên men rượu, sản xuất sữa chua, pho mát đều liên quan đến các phản ứng sinh hóa thuận nghịch.
-
Sản xuất vật liệu: Nhiều quá trình sản xuất vật liệu mới, như vật liệu nano, vật liệu sinh học, cũng dựa trên các phản ứng thuận nghịch.
Trong nghiên cứu
-
Hóa học hữu cơ: Phản ứng thuận nghịch được sử dụng rộng rãi trong tổng hợp hữu cơ để tạo ra các hợp chất mới và nghiên cứu các cơ chế phản ứng.
-
Sinh học: Nhiều quá trình sinh học liên quan đến các phản ứng thuận nghịch, chẳng hạn như quá trình hô hấp tế bào, quá trình quang hợp.
-
Y học: Nghiên cứu về các phản ứng thuận nghịch giúp phát triển các loại thuốc mới và hiểu rõ hơn về các quá trình bệnh lý.
-
Khoa học vật liệu: Nghiên cứu các phản ứng thuận nghịch giúp phát triển các vật liệu mới có tính chất đặc biệt.
Ý nghĩa của phản ứng thuận nghịch
-
Cân bằng tự nhiên: Nhiều quá trình tự nhiên trong vũ trụ đều đạt đến trạng thái cân bằng động. Việc hiểu rõ các phản ứng thuận nghịch giúp chúng ta hiểu rõ hơn về các quá trình này.
-
Phát triển công nghệ: Phản ứng thuận nghịch đóng vai trò quan trọng trong việc phát triển các công nghệ mới, như pin nhiên liệu, vật liệu nano,...
-
Bảo vệ môi trường: Việc hiểu rõ các phản ứng thuận nghịch giúp chúng ta tìm ra các giải pháp để xử lý ô nhiễm môi trường và bảo vệ tài nguyên thiên nhiên.
Phản ứng thuận nghịch, với đặc điểm đáng chú ý là khả năng chuyển đổi liên tục giữa chất tham gia và sản phẩm, không chỉ đơn thuần là một khái niệm hóa học. Nó có ảnh hưởng sâu rộng đến nhiều lĩnh vực trong đời sống, từ công nghệ sản xuất đến bản chất của các quá trình sinh học trong cơ thể. Thông qua việc nghiên cứu và áp dụng phản ứng này, chúng ta có thể tối ưu hóa quy trình sản xuất, phát triển các sản phẩm mới và đồng thời bảo vệ môi trường. Hóa chất Đông Á hi vọng rằng việc hiểu rõ về phản ứng thuận nghịch sẽ là chìa khóa giúp chúng ta khai thác tiềm năng của hóa học, góp phần xây dựng một thế giới bền vững và thịnh vượng.