Lưu huỳnh trioxit SO3 là gì?
Lưu huỳnh trioxit là một hợp chất hóa học với công thức SO₃. Nếu coi SO₂ như là "nhà" của lưu huỳnh, thì SO₃ chính là bức tranh hoàn thiện về những gì mà lưu huỳnh có thể đạt được khi kết hợp cùng oxy. Nó được coi là một trong những oxit axit mạnh nhất, một "sát thủ" trong thế giới hóa học, có khả năng phản ứng mãnh liệt với nước để tạo nên axit sulfuric - một trong những hóa chất cần thiết nhất trong nhiều lĩnh vực công nghiệp.
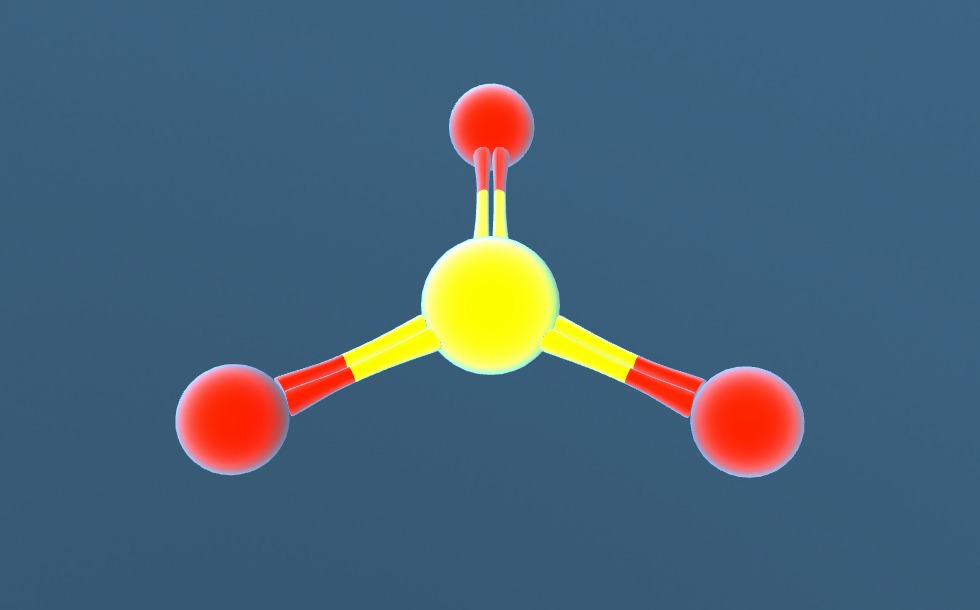
Lưu huỳnh trioxit SO3 là gì?
Dưới đây là bảng tóm lược thông tin về lưu huỳnh trioxit:
|
Thông tin
|
Chi tiết
|
|
Công thức hóa học
|
SO₃
|
|
Tình trạng
|
Chất lỏng không màu, mùi hăng
|
|
Tính chất hòa tan
|
Tan vô hạn trong nước
|
|
Sản phẩm phản ứng
|
Tạo ra axit sulfuric (H₂SO₄)
|
|
Ứng dụng chính
|
Sản xuất axit sulfuric
|
Cấu trúc phân tử SO₃ là gì?
Cấu trúc phân tử của SO₃ là một đề tài hấp dẫn trong hóa học, nơi mỗi nguyên tử đều đóng vai trò quan trọng trong việc xác định tính chất của hợp chất này. SO₃ có cấu trúc hình tam giác đều, với ba nguyên tử oxy bao quanh một nguyên tử lưu huỳnh ở chính trung tâm. Các góc liên kết giữa các nguyên tử oxy đạt 120 độ, cho thấy sự cân bằng tuyệt đối trong cấu trúc của nó.
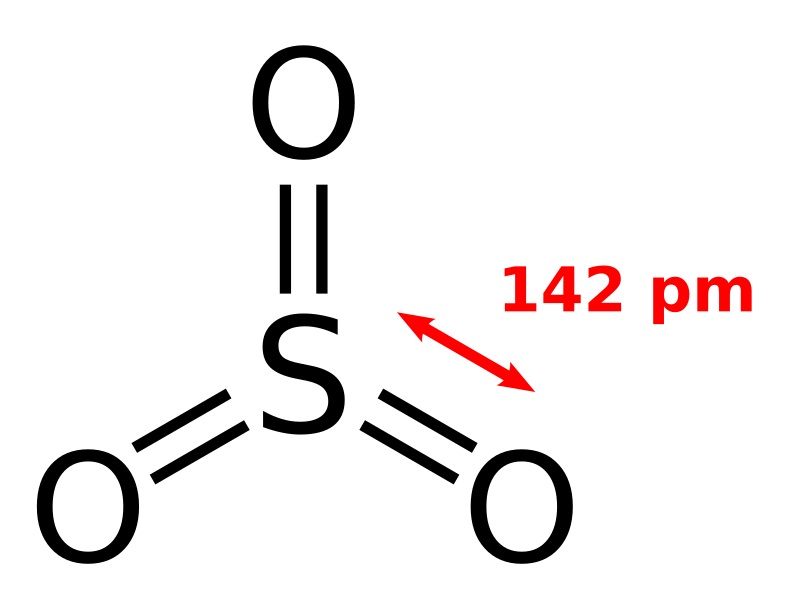
Cấu trúc phân tử SO₃
Nguyên tử lưu huỳnh trong SO₃ có hóa trị +6, điều này cho thấy lưu huỳnh đã kết hợp tối đa với oxy. Cấu trúc không phân cực của SO₃ khiến nó có khả năng hòa tan tốt trong nước, tạo ra axit sulfuric khi hình thành. Đây là một ví dụ điển hình cho sự khéo léo của thiên nhiên trong việc thiết kế các hợp chất hóa học.
Thông tin về cấu trúc SO₃ có thể được tóm lược như sau:
|
Thông tin
|
Chi tiết
|
|
Hình dạng
|
Tam giác đều
|
|
Góc liên kết
|
120 độ
|
|
Hóa trị lưu huỳnh
|
+6
|
|
Tính chất
|
Không phân cực
|
Tính chất của SO₃ là gì?
Lưu huỳnh trioxit sở hữu những tính chất vật lý và hóa học đặc biệt. Ở điều kiện tiêu chuẩn, SO₃ là một chất lỏng không màu, có mùi hăng đặc trưng, dễ dàng hấp thụ ẩm từ không khí. Điều này khiến SO₃ trở thành một chất cực kỳ nguy hiểm, vì chỉ cần tiếp xúc với hơi ẩm, nó sẽ phản ứng mạnh mẽ để tạo ra axit sulfuric.
SO₃ không chỉ mạnh về khả năng gây ăn mòn, mà còn có khả năng phản ứng mãnh liệt với nhiều chất khác nhau. Chất này được coi là nguyên liệu cơ bản trong sản xuất axit sulfuric, nhưng đồng thời, sự tương tác của nó với nước cũng có thể giải phóng một lượng nhiệt lớn, dẫn đến các hiện tượng hóa học phức tạp.
Dưới đây là bảng so sánh một số tính chất của SO₃:
|
Tính chất
|
Mô tả
|
|
Trạng thái
|
Chất lỏng không màu
|
|
Độ hòa tan
|
Tan vô hạn trong nước
|
|
Tính phản ứng
|
Tạo axit sulfuric với nước
|
|
Tính ăn mòn
|
Rất cao, cần xử lý cẩn thận
|
Ứng dụng của SO₃ trong công nghiệp
SO₃ có vai trò cực kỳ quan trọng trong ngành công nghiệp, đặc biệt trong quy trình sản xuất axit sulfuric. Axit sulfuric là một trong những hóa chất thiết yếu trong nhiều ngành công nghiệp, từ sản xuất phân bón, chế biến dầu khí, đến sản xuất hóa chất. SO₃ chính là cầu nối giúp hình thành axit sulfuric từ các thành phần cơ bản, với quy trình hiđrat hóa đơn giản nhưng hiệu quả.
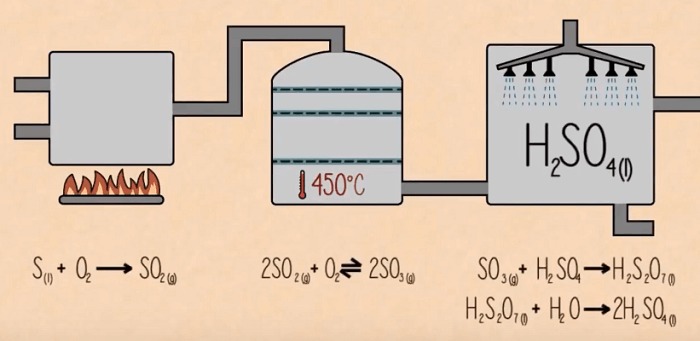
Ứng dụng của SO₃ trong công nghiệp
Ngoài việc sản xuất axit sulfuric, SO₃ còn được sử dụng như một chất oxi hóa mạnh trong nhiều phản ứng hóa học. Điều này mở ra nhiều khả năng cho các quy trình hóa học khác mà không thể thiếu sự hiện diện của SO₃. Một số ứng dụng khác của SO₃ bao gồm sản xuất thionyl chloride và các hợp chất hữu cơ khác.
Thông tin tóm tắt về ứng dụng của SO₃:
|
Ứng dụng
|
Mô tả
|
|
Sản xuất axit sulfuric
|
Hợp chất quan trọng trong hóa chất
|
|
Chất oxi hóa
|
Tham gia trong nhiều phản ứng hóa học
|
|
Sản xuất hóa chất khác
|
Tạo ra các hợp chất hữu cơ khác
|
Lưu ý khi sử dụng SO₃
Khi làm việc với SO₃, việc tuân thủ các quy định an toàn là rất cần thiết. SO₃ có tính ăn mòn cao, do đó, sự tiếp xúc trực tiếp với chất này có thể gây ra những tổn thương nghiêm trọng cho người làm việc. Điều này không chỉ đúng với da mà còn cả các bộ phận hô hấp nếu hít phải hơi SO₃.
Người làm việc với SO₃ cần tuân theo những quy trình bảo hộ cá nhân như đeo găng tay, kính bảo hộ và mặt nạ phòng độc. Điều kiện làm việc cần đảm bảo thông gió tốt, tránh sự tích tụ của hơi SO₃ trong không khí. Ngoài ra, các thiết bị chứa SO₃ cần được làm từ vật liệu không phản ứng với chất này để tránh hiện tượng ăn mòn.
Các lưu ý khi sử dụng SO₃ có thể được tóm lược dưới đây:
|
Lưu ý
|
Mô tả
|
|
Bảo hộ cá nhân
|
Đeo găng tay, kính và mặt nạ
|
|
Môi trường làm việc
|
Thông gió tốt
|
|
Chất liệu chứa
|
Không phản ứng với SO₃
|
|
Xử lý sự cố
|
Sử dụng biện pháp hút và làm sạch
|
Tác động của SO₃ đến môi trường
Lưu huỳnh trioxit (SO₃) là một hợp chất hóa học vô cùng quan trọng trong công nghiệp, nhưng đồng thời cũng là một trong những chất gây ô nhiễm không khí nghiêm trọng. Khi thải ra môi trường, SO₃ gây ra nhiều tác động tiêu cực, ảnh hưởng đến cả con người và hệ sinh thái.
Cơ chế gây ô nhiễm

Khí SO₃ gây ô nhiễm môi trường
● Tạo thành mưa axit: Khi SO₃ tiếp xúc với hơi nước trong không khí, nó sẽ kết hợp tạo thành axit sulfuric (H₂SO₄). Axit sulfuric này hòa tan trong nước mưa, tạo thành mưa axit.
● Làm tăng độ chua của đất và nước: Mưa axit làm tăng độ chua của đất và nước, gây hại cho thực vật, động vật thủy sinh và làm suy thoái đất.
● Gây ăn mòn các công trình: Axit sulfuric có tính ăn mòn cao, gây hư hại các công trình xây dựng, tượng đài, và các vật liệu kim loại.
● Ảnh hưởng đến sức khỏe con người: Khi hít phải khí SO₃, con người có thể bị các vấn đề về đường hô hấp như ho, khó thở, viêm phế quản. Ở nồng độ cao, SO₃ có thể gây tổn thương phổi nghiêm trọng.
Các nguồn phát thải SO₃ chính
● Ngành công nghiệp: Các nhà máy nhiệt điện sử dụng nhiên liệu hóa thạch như than đá, dầu là nguồn phát thải SO₃ lớn nhất. Ngoài ra, các ngành công nghiệp luyện kim, hóa chất cũng thải ra một lượng đáng kể SO₃.
● Phương tiện giao thông: Khí thải từ các phương tiện giao thông chạy bằng nhiên liệu hóa thạch cũng chứa một lượng nhỏ SO₃.
Biện pháp giảm thiểu ô nhiễm môi trường do SO₃ gây ra
Để giảm thiểu tác động của SO₃ đến môi trường, chúng ta cần thực hiện một số biện pháp sau:
Cải thiện công nghệ
○ Sử dụng các công nghệ lọc khí thải hiệu quả để loại bỏ SO₃ trước khi thải ra môi trường.
○ Ứng dụng các công nghệ đốt cháy nhiên liệu sạch hơn, giảm lượng SO₃ thải ra.
Phát triển năng lượng sạch
○ Tăng cường sử dụng các nguồn năng lượng tái tạo như năng lượng mặt trời, gió, thủy điện để thay thế nhiên liệu hóa thạch.
Cải thiện chất lượng nhiên liệu
○ Sử dụng các loại nhiên liệu có hàm lượng lưu huỳnh thấp.
Củng cố pháp luật và chính sách
○ Ban hành các quy định nghiêm ngặt về tiêu chuẩn khí thải.
○ Tăng cường kiểm soát và xử lý các cơ sở sản xuất gây ô nhiễm.
Tóm lại, SO₃ là một chất gây ô nhiễm không khí nghiêm trọng, gây ra nhiều tác hại đến môi trường và sức khỏe con người. Để bảo vệ môi trường và sức khỏe, chúng ta cần có những biện pháp mạnh mẽ để giảm thiểu lượng SO₃ thải ra môi trường.
Cảm ơn các bạn đã theo dõi bài viết của chúng tôi để hiểu rõ thêm về SO₃ là gì. Hãy truy cập website dongachem.vn thường xuyên để cập nhật thêm nhiều bài viết bổ ích khác nữa các bạn nhé!