Axit Photphoric với công thức hóa học là H3PO4 được xem là một hóa chất có hại nhưng lại đóng vai trò quan trọng đối với nhiều ngành nghề hiện nay. Vậy, axit Photphoric là gì? Những đặc điểm nổi bật và ứng dụng quan trọng của hóa chất này là như thế nào? Hãy cùng tìm hiểu một cách chi tiết về hóa chất axit Photphoric trong nội dung tiếp theo sau đây.
1. Giới thiệu axit Photphoric là gì?
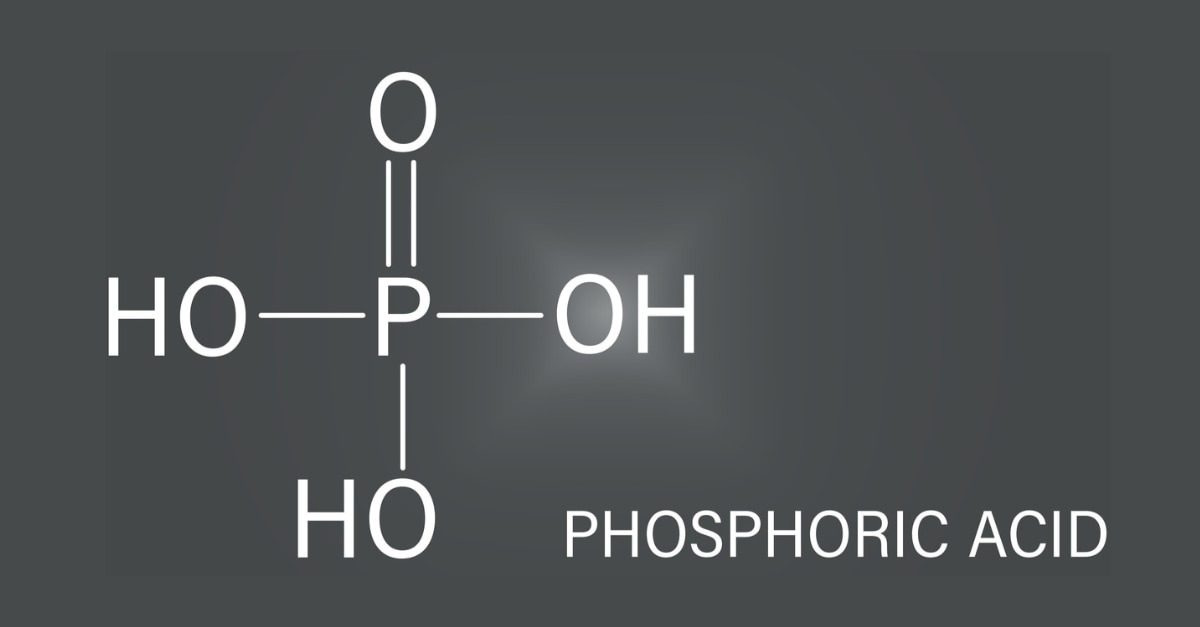
Giới thiệu axit Photphoric là gì?
Axit Photphoric còn được gọi với những cái tên khác, như là: Trihiđroxiđophotpho, axit orthophosphoric, axit phosphoric. Công thức của axit photphoric là H3PO4. Cấu tạo phân tử của axit photphoric gồm có 3 nấc phân li, 3 phân tử hidro kết hợp với gốc PO4.
Điểm đặc biệt của cấu trúc tinh thể axit photphoric chính là có tứ diện PO4 được liên kết với nhau bằng hidro.
Có thể nói, loại axit này có nhiều ứng dụng quan trọng đối với nhiều ngành công nghiệp cũng như đời sống con người hiện đại.
2. Các đặc trưng tính chất H3PO4
Ở phần trên, chúng ta đã tìm hiểu chi tiết axit photphoric là gì. Tiếp theo đây, chúng ta sẽ tiếp tục nghiên cứu những tính chất lý hóa đặc trưng của hóa chất H3PO4 này.
Tính chất vật lý
Sau đây là một số tính chất vật lý của axit photphoric đặc trưng mà chúng ta không thể bỏ qua:
-
Loại axit này thường tồn tại ở 2 dạng là thể rắn không màu và thể lỏng không màu, trong suốt, có vị chua đặc trưng
-
Khối lượng riêng của axit là 1.87 g/cm3, nhiệt độ nóng chảy là 42.35 độ C (trường hợp axit nằm ở dạng H3PO4.H2O sẽ có nhiệt độ nóng chảy là 29.32 độ C).
-
Đặc biệt, nhiệt độ phân hủy của axit photphoric là 213 độ C, có thể tan vô hạn trong nước và etanol.
Tính chất hóa học
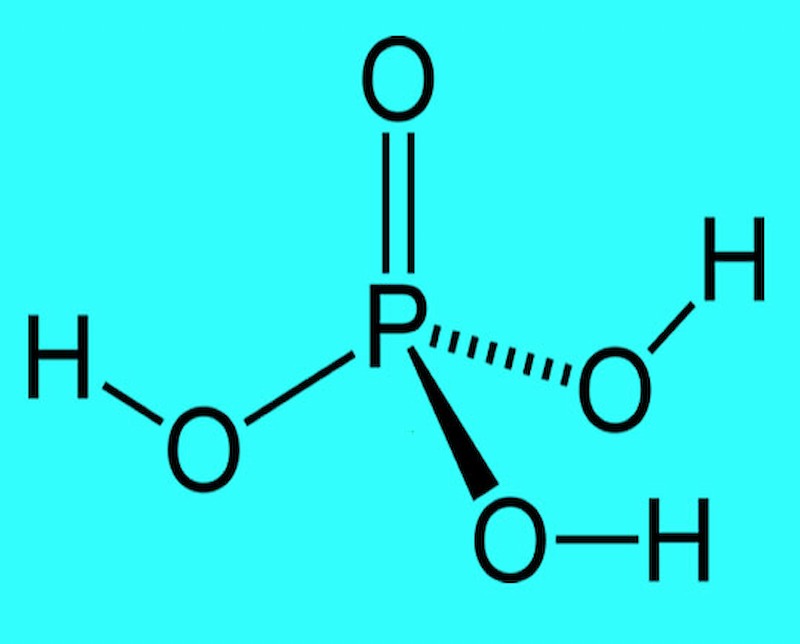
Tính chất hóa học axit photphoric
Tính chất hóa học của axit photphoric có rất nhiều phản ứng thú vị. Có thể kể ra một số phản ứng hóa học đặc trưng như sau:
H3PO4 ↔ H+ + H2PO4-
H2PO4- ↔ H+ + HPO42-
HPO42- ↔ H+ + PO43-
2H3PO4 + 3Na2O → 2Na3PO4 + 3H2O
Ví dụ như:
KOH + H3PO4 → KH2PO4 + H2O
2KOH + H3PO4 → K2HPO4 + 2H2O
3KOH + H3PO4 → K3PO4 + 3H2O
2H3PO4 + 3Mg → Mg3(PO4)2 + 3H2
Tác dụng với muối tạo ra một loại muối và axit mới
H3PO4 + 3AgNO3 → 3HNO3 + Ag3PO4
Axit H3PO4 với P có mức oxi hóa là +5. Đây là mức oxi hóa cao nhất, tuy nhiên, bản thân H3PO4 lại không có tính oxi hóa như HNO3. Lý do cho tình trạng này là vì nguyên tử P có bán kính lớn hơn với bán kính của N nên khiến mật độ điện dương trên P nhỏ hơn, từ đó dẫn đến khả năng nhận e kém hơn.
Khi ở trong môi trường nhiệt độ từ 200 đến 250 độ C, axit Photphoric sẽ nhiệt phân theo phản ứng hóa học sau đây:
2H3PO4 → H4P2O7 + H2O
Trong môi trường có nhiệt độ từ 400 đến 500 độ C, dung dịch axit Photphoric sẽ nhiệt phân dựa trên phản ứng hóa học:
H4P2O7 → 2HPO3 + H2O
3. 2 cách điều chế axit Photphoric

cách điều chế axit Photphoric
Ngày nay, quá trình điều chế axit photphoric thường theo 2 cách sau đây
Điều chế H3PO4 tại phòng thí nghiệm
Cách điều chế axit photphoric trong phòng thí nghiệm sẽ dựa vào phản ứng oxi hóa P ở nhiệt độ cao tạo thành. Phản ứng hóa học của quá trình này diễn ra như sau:
P + 5HNO3 -> H3PO4 + 5NO2 + H2O
Điều chế axit photphoric trong công nghiệp
Để điều chế axit photphoric trong công nghiệp, chúng ta sẽ dựa vào hai phương pháp chính theo quá trình nhiệt hay quá trình ẩm ướt.
Trong đó, quá trình nhiệt còn được gọi là phương pháp khô. Với cách này, H3PO3 sẽ được tạo ra bằng cách đốt P nguyên tố, từ đó tạo ra hợp chất Photpho pentaoxit. Hợp chất tạo ra đem hòa tan với axit photphoric với nồng độ loãng. Tiếp theo sẽ tạo phản ứng đốt Photpho bên trong lò điện giúp loại bỏ toàn bộ tạp chất để tạo được H3PO4 tinh khiết.
Các phản ứng hóa học sẽ diễn ra trình tự như sau:
P → P2O5 → H3PO4
4P + 5O2 → 2P2O5
P2O5 + 3H2O → 2H3PO4
Phương pháp thứ hai gọi là quá trình ẩm ướt hay còn có cái tên khác là phương pháp trích ly. Cách này sử dụng axit sunfuric phân hủy khoáng Calcium Phosphate. Đây là loại khoáng thường xuất hiện trong tự nhiên ở tại một số quặng apatit.
Công thức hóa học được diễn ra:
Ca3(PO4)2 + 3H2SO4 đặc → 3CaSO4 + 2H3PO4 (t0)
4. Ứng dụng của axit photphoric trong sản xuất và đời sống
Ứng dụng của axit photphoric đối với nhiều ngành nghề hiện nay là rất to lớn, đặc biệt là trong ngành công nghiệp và nông nghiệp.
Ứng dụng của H3PO4 trong công nghiệp
Có thể kể ra một số ứng dụng của H3PO4 trong ngành công nghiệp hiện đại như sau:
-
Đóng vai trò là chất phụ gia để sản xuất một số đồ uống, thạch rau câu, mứt, pho mát. Ngoài ra, H3PO4 còn có công dụng tạo hương thơm và độ đậm đà cho một số loại thực phẩm. Để làm được điều này, người ta cho H3PO4 kết hợp với Hfcs đã xử lý enzyme để tạo thêm vị ngọt cho thực phẩm.
-
Là nguyên liệu quan trọng trong quá trình sản xuất xi mạ, thủy tinh gạch men, chất giặt tẩy, xử lý nước, chất chống ăn mòn kim loại và chất tẩm gỗ chống cháy,...
-
Có công dụng làm chậm quá trình phát triển của một số loại nấm mốc và vi khuẩn trong đường. Đó cũng là lý do người ta sử dụng axit photphoric để làm chất bảo quản thực phẩm.
-
Là nguyên liệu để sản xuất các sản phẩm từ sữa. Một công dụng của muối từ axit photphoric có thể làm thay đổi protein, độ pH, giúp cải thiện hiệu quả chất lượng của sữa.
Ứng dụng axit photphoric trong nông nghiệp
Đối với ngành sản xuất nông nghiệp, H3PO4 đậm đặc có hàm lượng P2O5 từ 70 đến 75%. Đây là nguyên liệu quan trọng, không thể thiếu được cho quy trình sản xuất phân bón, thuốc trừ sâu, phân lân,...
5. Lưu ý khi sử dụng axit H3PO4
Rất nhiều người băn khoăn: Axit Photphoric có độc không? Câu trả lời chính xác là H3PO4 là một loại axit độc, có thể gây nguy hiểm đến sức khỏe nghiêm trọng nếu tiếp xúc. Chính vì vậy, trong quá trình sử dụng axit H3PO4, chúng ta cần lưu ý một số điểm sau đây:
-
H3PO4 thường được sử dụng như là một nguyên liệu làm nước ngọt. Tuy nhiên, bản chất của loại axit này có thể làm giảm mật độ xương của con người. Chính vì vậy, các chuyên gia thường khuyên chúng ta nên hạn chế uống quá nhiều nước ngọt hàng ngày.
-
P có trong H3PO4 có thể làm con người mắc một số bệnh, như là: đường tiết niệu, sỏi thận,... Chính vì vậy, khi sử dụng những thực phẩm mà trong thành phần có sử dụng axit này cần phải lưu ý và hạn chế dùng quá nhiều.
Có thể nói, thông qua quá trình tìm hiểu axit photphoric là gì, chúng ta đã thấy được bản chất, đặc tính của loại hóa chất này, từ đó khám phá ra những ứng dụng quan trọng của axit H3PO4 đối với một số ngành nghề hiện nay.